Linus Carl Pauling, nasceu nos Estados Unidos da América em Portland, no dia 28 de Fevereiro de 1901, tendo falecido a 19 de Agosto de 1994, em Big Sur. Foi um químico quântico e um bioquímico, apesar de também ser reconhecido como cristalógrafo, biólogo molecular e pesquisador médico.

Linus Pauling é amplamente reconhecido como um dos principais químicos do século XX. Foi pioneiro na aplicação da Mecânica Quântica em Química e, recebeu o Nobel de Química em 1954, pelo seu trabalho relativo à natureza das ligações químicas. Também efetuou importantes contribuições relativas à determinação da estrutura de proteínas e cristais, sendo considerado um dos fundadores da Biologia Molecular. Durante as suas investigações esteve perto de descobrir a estrutura em hélice dupla do ADN, descoberta essa efetuada mais tarde por James Watson e Francis Crick, em 1953.
Ele também é reconhecido como um académico versátil, devido à sua intervenção e perícia em campos diversos como a Química Inorgânica, Química Orgânica, Metalurgia, Imunologia, Anestesiologia, Psicologia e Radioatividade.
Pauling recebeu o Nobel da Paz de 1962, pela sua campanha contra os testes nucleares e é a única personalidade a ter recebido dois Prémios Nobel não compartilhados. As outras personalidades que receberam dois Prémios Nobel foram Marie Curie (Física e Química), John Bardeen (ambos em Física) e Frederick Sanger (ambos em Química). Mais tarde na sua carreira científica, advogou o uso em maiores proporções, em dietas, de vitamina C e outros nutrientes. Generalizou as suas ideias nesta área com vista a definir Medicina Ortomolecular, que ainda é vista como método não ortodoxo pela Medicina convencional. Pauling popularizou as suas ideias, análises, pesquisa e visões em vários livros de sucesso, mas controversos, sobre a temática da vitamina C e Medicina Ortomolecular.
Linus Pauling era filho de Hermann Heinrich Wilhelm Pauling, de ascendência alemã, e de Lucy Isabelle Darling. O seu pai era um farmacêutico que, sem ter êxito comercial, fez com que a sua família percorresse diferentes lugares do estado do Oregon. Quando o seu pai morreu, em 1910, Lucy Isabelle teve que criar sozinha Linus e as suas duas irmãs, Pauline e Frances Lucille. A família voltaria mais tarde a reinstalar-se em Portland.
Durante a infância, Linus foi um leitor voraz, tanto que o seu pai chegou a escrever para um periódico local, pedindo sugestões de livros para mantê-lo ocupado. Um dos seus amigos, Lloyd Jeffress, tinha um pequeno laboratório químico na sua habitação; e as experiências levadas a cabo neste laboratório despertaram o interesse de Pauling em se tornar um engenheiro químico. Durante os seus estudos, Pauling continuava com as experiências de química, procurando a maioria dos materiais e equipamentos utilizados numa fábrica abandonada que existia perto do local onde o seu avô tinha trabalhado como guarda noturno.
As más classificações que Pauling obteve em história dos Estados Unidos impediram-no de obter, nessa altura, o seu diploma de ensino médio. A escola concedeu-lhe o diploma quarenta e cinco anos mais tarde, depois de ter ganho os seus dois Prémios Nobel.
Em 1917, Pauling ingressou na Universidade Agrícola do Oregon ("OAC", denominada atualmente de Universidade Estadual do Oregon), em Corvallis. Paralelamente aos seus estudos, Linus Pauling teve que trabalhar a tempo inteiro, devido às suas necessidades financeiras. Entre os empregos que teve, encontram-se o de distribuidor de leite, projeccionista num cinema e como trabalhador num estaleiro naval. No começo do seu segundo ano de estudos, Pauling propôs-se a encontrar emprego em Portland para poder ajudar financeiramente a sua mãe. Na mesma altura, na Universidade, propuseram-lhe que aceitasse uma cátedra de química analítica quantitativa (um curso que ele mesmo acabava de concluir como estudante), que lhe permitiria, ao mesmo tempo, continuar os seus estudos.
Durante os seus dois últimos anos na OAC,Pauling estudou o trabalho de Lewis e Langmuir sobre a configuração electrónica dos átomos, assim como a forma como estes se ligavam para formar moléculas. Neste momento, decidiu seguir uma carreira de investigação, concentrando-se na compreensão da relação da estrutura atómica da matéria com as suas propriedades físicas e químicas, o que o levaria a converter-se num dos pioneiros da química quântica. Na OAC, teve a oportunidade de realizar as suas primeiras investigações respeitantes ao efeito que um campo magnético exerce sobre a orientação de um cristal de ferro.
Pauling graduou-se como Bachelor of Science, em 1922, na área de engenharia de processos. Imediatamente, procurou continuar os estudos com uma pós-graduação no California Institute of Technology (Caltech) em Pasadena. Em busca do doutoramento, Pauling investigou a utilização da difração de raios-X, na determinação das estrutura dos cristais. Durante os seus três anos em Caltech, Pauling publicou sete artigos sobre a estrutura cristalina dos minerais. O primeiro deles foi publicado na revista Journal of the American Chemical Society, e tratava a estrutura da molibdenita, MoS2. Linus Pauling recebeu o doutoramento summa cum laude em 1925.
A 17 de Junho de 1923, Pauling casou-se com Ava Helen Miller, com quem teve três filhos e uma filha. O casal tinha-se conhecido na OAC, quando Pauling cursava o último ano de estudos. Miller foi aluna de Pauling no curso "Química para estudantes de Economia Doméstica".
O diagrama de Linus Pauling ou diagrama de Pauling é um diagrama feito químico para auxiliar na distribuição dos eletrões pelos vários subníveis da eletrosfera.
Os subníveis são designados por letras:
s (sharp = nítido),
p (principal),
d (diffuse = difuso),
f (fundamental).
Os eletrões podem distribuir-se por sete níveis (ou camadas) diferentes. Cada um deles é composto por um ou mais subníveis de energia (ou subcamadas).
A camada K é composta pelo subnível s;
A camada L é composta pelos subníveis s e p;
A camada M é composta pelos subníveis s, p e d;
A camada N é composta pelos subníveis s, p, d e f;
A camada O é composta pelos subníveis s, p, d e f;
A camada P é composta pelos subníveis s, p e d;
A camada Q é composta pelos subníveis s e p.
O número máximo de eletrões permitido em cada uma das orbitais é:
s - 2 eletrões
p - 6 eletrões
d - 10 eletrões
f - 14 eletrões
g - 18 eletrões
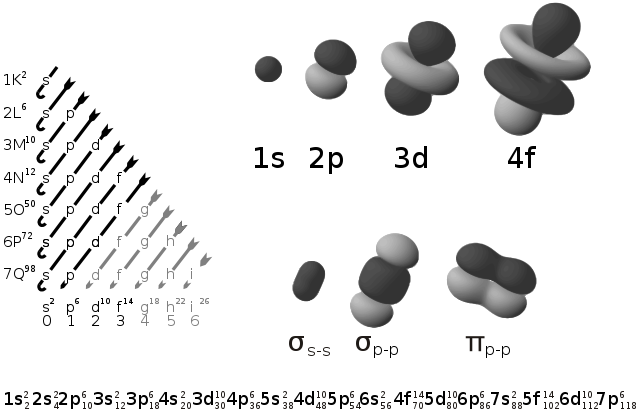
O diagrama pode ser apresentado assim (tal como podes ver na figura ao lado - as setas indicam o sentido do preenchimento):
K 1s2
L 2s2 2p6
M 3s2 3p6 3d10
N 4s2 4p6 4d10 4f14
O 5s2 5p6 5d10 5f14
P 6s2 6p6 6d10
Q 7s2 7p6
A ordem do diagrama (ver figura) que se lê é: 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p6, 5s2, 4d10, 5p6, 6s2, 4f14, 5d10, 6p6, 7s2, 5f14, 6d10, 7p6.
Confuso ?
O número indica o nível de energia, e a letra, a orbital. O expoente diz quantos eletrões pode levar essa orbital.
Ex: 1s2 - Primeiro nível (camada K) onde se encontra uma orbital s (ou subnível), que pode ser preenchida com um máximo de 2 eletrões