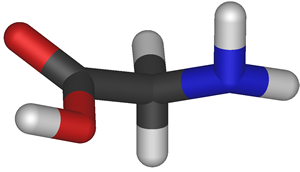
É um cristal branco ou pó cristalino, sem odor e de sabor adocicado. É bastante solúvel em água e ácido fórmico e praticamente insolúvel em etanol. A Glicina é fabricada pela síntese química a partir de formaldeído ou ácido monocloroacético e amoníaco.
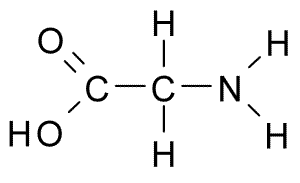
A glicina (do grego glykos, "doce", nome devido ao seu sabor adocicado) é um dos aminoácidos codificados pelo código genético, sendo portanto um dos componentes das proteínas dos seres vivos.
Devido à sua simplicidade estrutural, este aminoácido tende a ser conservado evolucionariamente em proteínas como o citocromo c, a mioglobina e a hemoglobina. A glicina é o único aminoácido que não apresenta atividade ótica. A maioria das proteínas possui pequenas quantidades de glicina; o colagénio é uma excepção à regra, constituíndo a glicina cerca de um terço da sua estrutura primária. A presença de glicina inibe a formação de hélices alfa mas facilita a formação de voltas beta na estrutura secundária de proteínas, por ser um aminoácido que apresenta um alto grau de flexibilidade quando integrado numa cadeia polipeptídica.
Apesar de ser um aminoácido apolar, a sua cadeia lateral (um átomo de hidrogénio) é demasiado curta para participar em interacções hidrofóbicas. No entanto, a glicina pode, em determinadas enzimas como a piruvato:formato liase, ser convertida a radical glicilo através da retirada desse átomo de hidrogénio, sendo este radical importante para a catálise enzimática, embora instável e destruído na presença de oxigénio.
A glicina não é um aminoácido essencial na dieta humana, já que é sintetizado pelo organismo a partir do aminoácido serina numa reação catalizada pela enzima serina hidroximetiltransferase.
A glicina serve de precursor a diversas espécies químicas. O ácido aminolevulínico, precursor chave das porfirinas, é sintetizado in vivo a partir de glicina e succinil-coenzima A. A glicina fornece também o bloco C2N central a todas as purinas. Uma das vias de degradação do aminoácido treonina passa pela sua conversão a glicina, embora esta via metabólica seja relativamente pouco importante no metabolismo humano. É ainda precursor na via biossintética da fosfocreatina.
A glicina é um neurotransmissor inibitório no sistema nervoso central, especialmente a nível da medula espinal, tronco cerebral e retina. Quando recetores de glicina são ativados, o anião cloreto entra no neurónio através de recetores ionotrópicos, causando um potencial pós-sináptico inibitório. A estricnina atua como antagonista nos recetores ionotrópicos de glicina. A glicina é, juntamente com o glutamato, um co-agonista de recetores NMDA; esta ação facilita a atividade excitatória dos recetores glutaminérgicos, em contraste com a atividade inibitória da glicina.
Nome sistemático (IUPAC): Ácido Aminoetanóico
Abreviatura/Símbolo: G / Gly
Fórmula química: C2H5NO2
Massa Molecular: 75,06
Ponto de fusão: 233 °C (decompõe-se)
Densidade: 1,1607 g/cm3
Imagem "Glicina 3d". Licenciado sob CC BY-SA 3.0, via Wikimedia Commons